構造有機化学と医薬化学の両者に携わる研究室です。一見、別の分野に見える2つの研究分野ですが、分子の立体構造、特性を詳細に解析し、その知見をもとに、新規な生理活性物質の設計・合成を行うという点で、2つの研究テーマは根底でつながっています。主に芳香族アミドとその関連化合物に着目し、研究を行なっています。
1.アミドおよび関連官能基の立体特性を活かしたユニークな芳香族分子構築
分子を構成する様々な官能基、部分構造の中でも、アミド結合はタンパク質の基本骨格でもあり、また多くの生理活性物質、分子集合体等の鍵構造として重要な機能を果たしています。一般に、アミド結合及び類縁官能基であるウレアやグアニジンは、水素結合部位に富んだグループとして、分子内もしくは分子間の電子的相互作用を意図して分子構築に用いられています。一方、これら部分二重結合性を持つ官能基の立体挙動が分子の三次元構造や物性に関わることも多々みられます。本研究室では、芳香族アミド類が「N-メチル化されるとシス型構造を優先する」ことに着目し、その一般性を示してきました(図1)1)。この立体特性は一見単純ではありますが、この性質を用いて、例えば、芳香族多層構造やらせん構造といったユニークな立体構造や動的挙動を有する芳香族分子の構築が可能であり、さらに触媒や液晶などの機能性分子への応用も進めています。
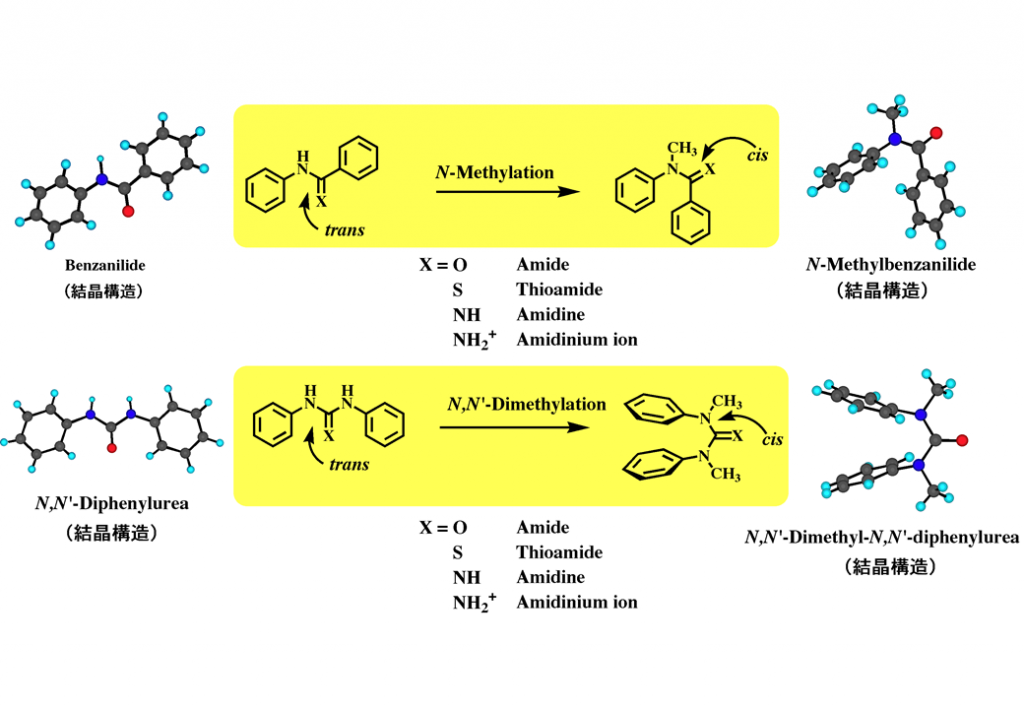
1) Tanatani, A. et al. J. Synth. Org. Chem., Jpn 2000, 58, 556-567.
1)芳香族多層構造と動的らせん分子の構築
上述の芳香族ウレアやグアニジンのシス型構造では、2つの芳香環が向き合った構造をとります。さらに複数の芳香環を複数のシス型ウレアやグアニジノ基で連結すると芳香属多層構造が構築できます(図2)2)。リンカーがグアニジノ基の場合は、分子が水溶性となり、興味深いことに、多層グアニジン5PGは二本鎖DNAのマイナーグルーブにぴったりとはまり込む性質を持っていました。 また、化合物5MUのようにメタ位で連結した層状分子の場合は、すべての軸不斉がRまたはSにそろった、らせん様構造を形成しています。 このらせん様構造は溶液中では右巻きと左巻きの分子間で非常に速い平衡下にあります3,4)。
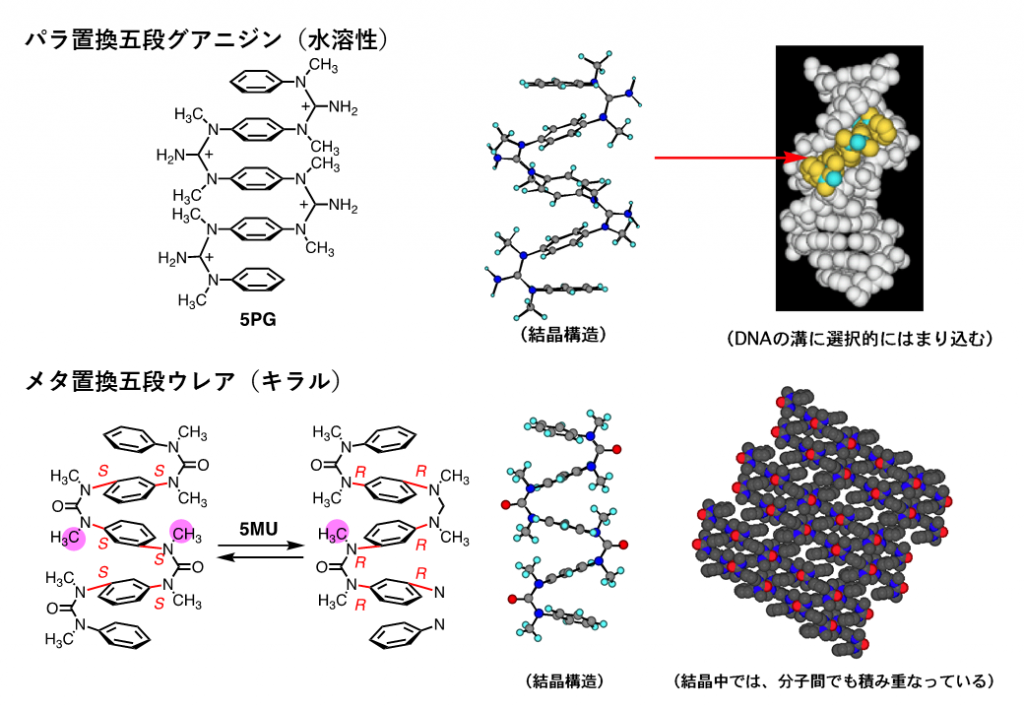
2) Tanatani, A. et al. J. Am. Chem. Soc. 1998, 120, 6433-6442.
3) Kudo, M. et al. J. Org. Chem. 2009, 74, 8154-8163.
4) Kudo, M.; Tanatani, A. New J. Chem. 2015, 39, 3190-3196.
2)様々な芳香環を有するオリゴアミドフォルダマーの構築
シス型構造をとるN-メチルベンズアニリドをモノマー単位としてオリゴマーやポリマーを構築すると、らせん構造をとります(図3)5)。ポリアミド1はモノマー分子2から連鎖重縮合反応で分子量幅の狭いポリマーとして合成できますが、窒素原子上にキラルな側鎖を有しており、一方向巻きのらせん構造を優先して取ります。どちらの巻き方になっているかはUV/CDスペクトルの実験的および計算科学的解析により同定することができました。
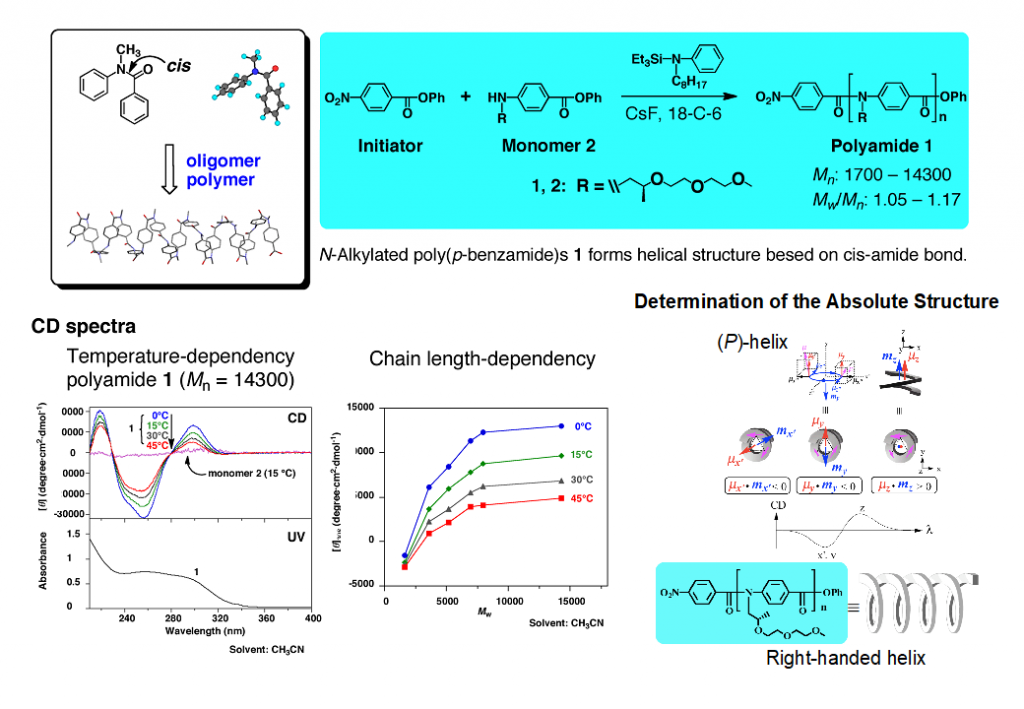
5)Tanatani, A. et al. J. Am. Chem. Soc. 2005, 127, 8553-8561.
このらせん構造をとるオリゴアミドは、ベンゼン環以外の芳香環でも同様に構築することができます。実際に五員環複素芳香環であるN-メチルピロール環とベンゼン環をN -アルキル化アミドで交互に連結させた化合物3が結晶中においてらせんの部分構造の形状をとることを明らかにしました(図4)6)。本化合物は、アミド結合の窒素原子上に光学活性な側鎖を持つことで、CDスペクトルが温度依存性、鎖長依存性を示し、動的なフォールディング構造をとることがわかりました。
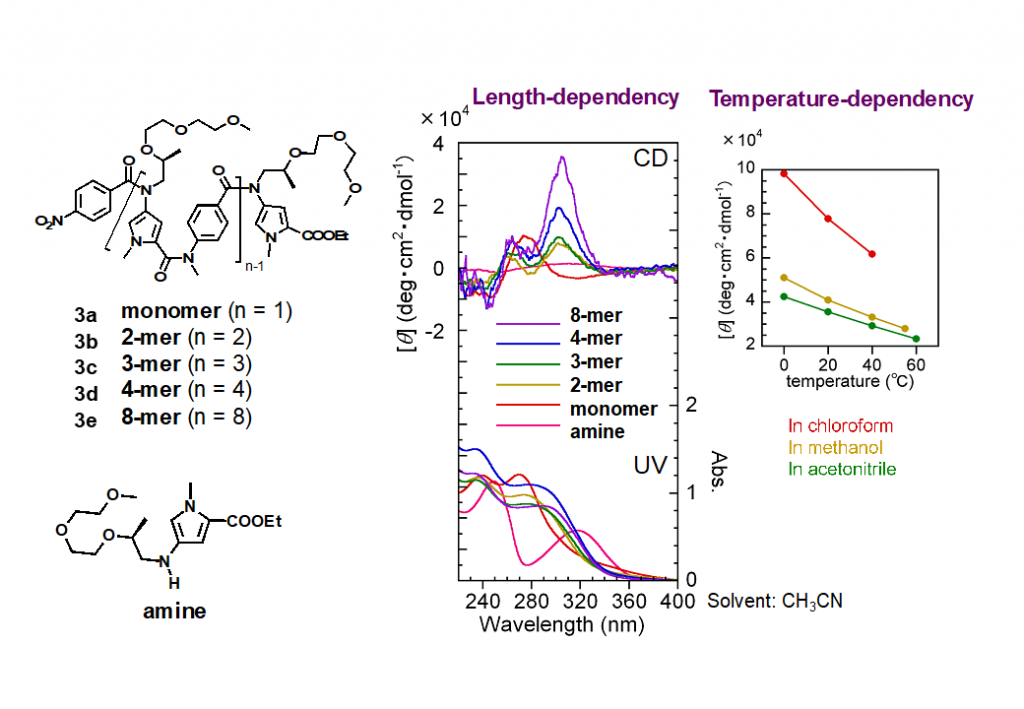
6)Tojo, Y. et al. J. Org. Chem. 2018, 83, 4606-4617.
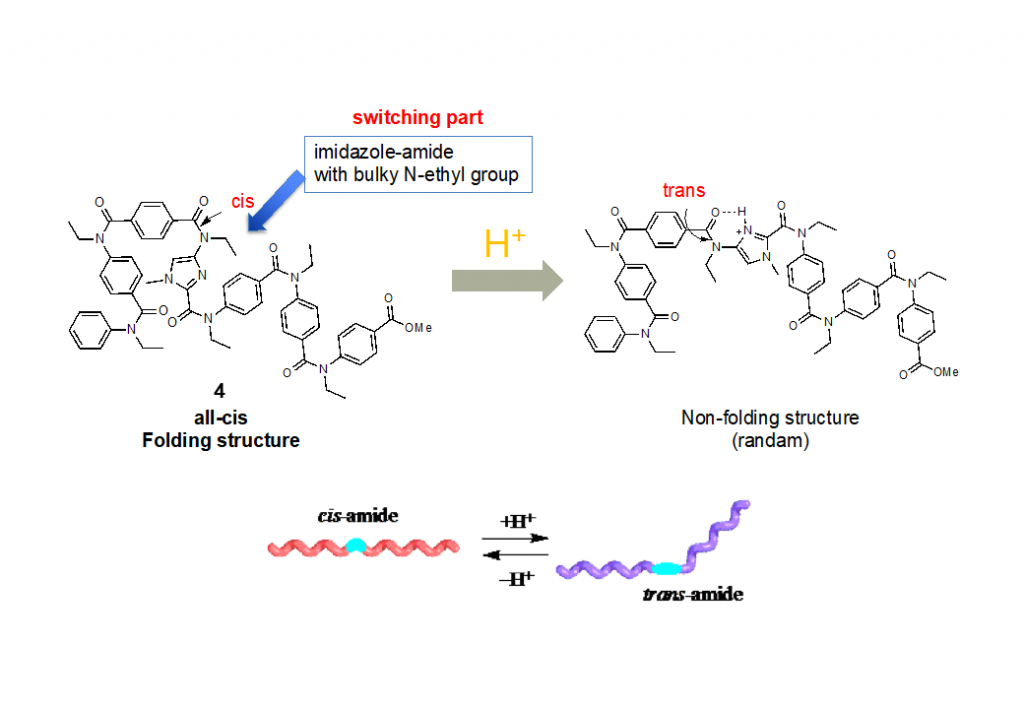
さらに五員環複素芳香環をピロール環からイミダゾール環へと展開したオリゴマー4では、イミダゾール環へのプロトン化によりシス型とトランス型間の立体転換を引き起こし、それに伴って、動的に構造を変化させるオリゴマーを構築することに成功しています(図5)。
3)らせん状層状ウレア分子のキラリティーを利用した不斉有機分子触媒への展開
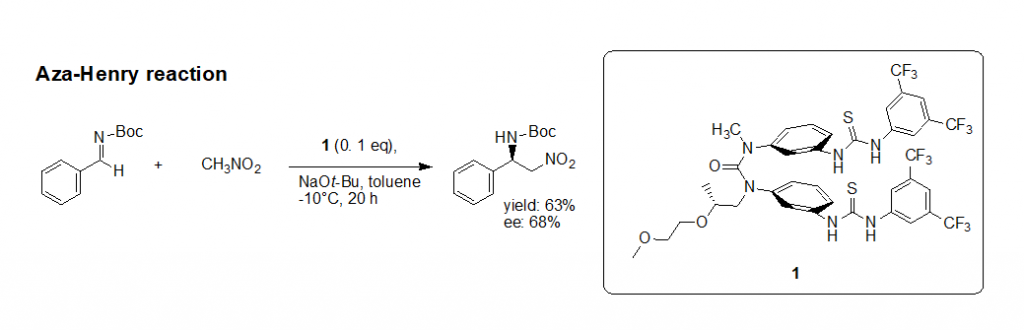
上記で紹介したシス型芳香族ウレアは動的らせん分子としての性質を持っています。このキラリティーの特性を利用して、不斉有機分子触媒の構築を検討しています。例えば、光学活性側鎖を導入したウレア分子5が不斉アザヘンリー反応の触媒として機能することをみいだしました(図6)。
4)スクアルアミドの特徴を活かした新たな分子構築への展開
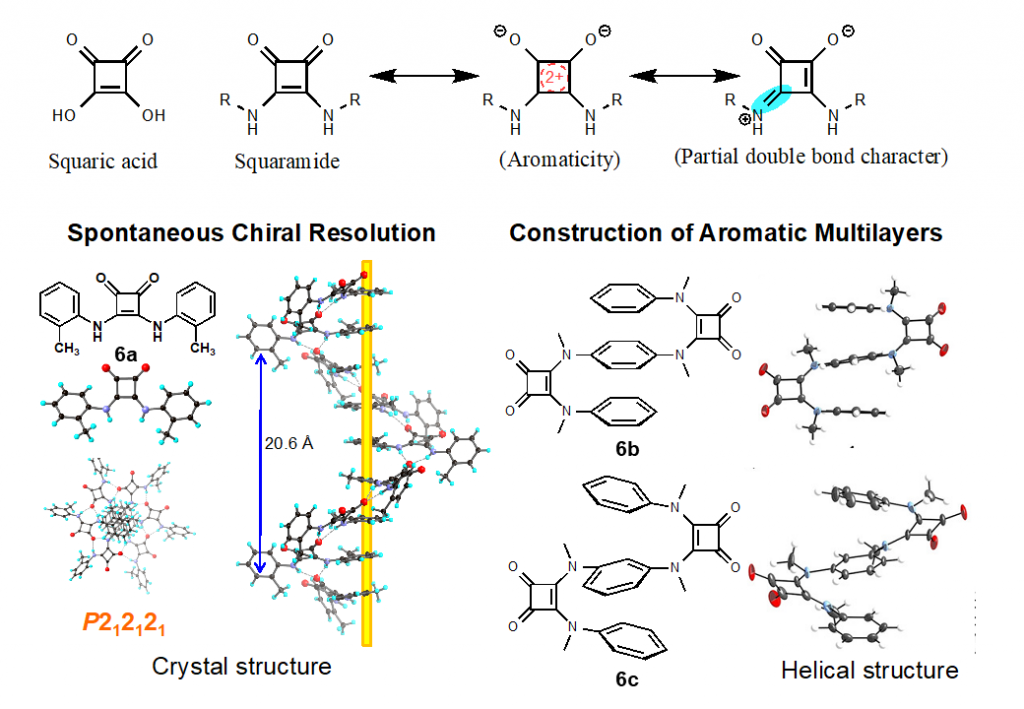
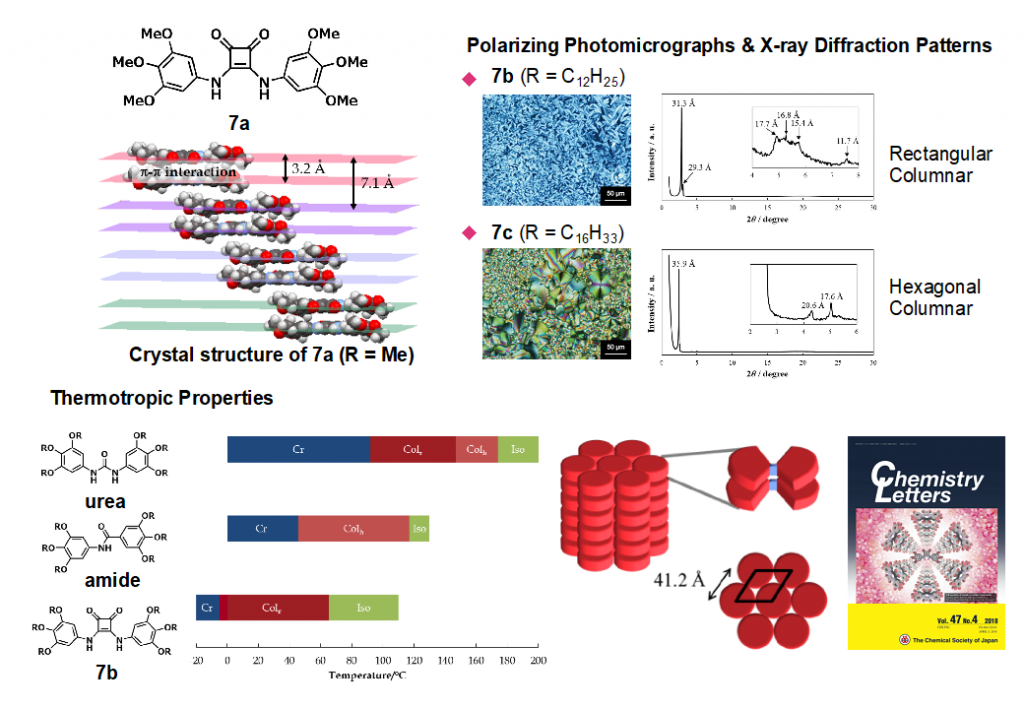
スクアルアミドは四員環構造を持つスクアリン酸とアミンを縮合させた化合物ですが、C-N結合が部分二重結合性を持ち、シス型―トランス型異性体を生じるなど、立体的な性質がアミドやウレアと類似しています。医薬化学分野ではスクアルアミドはウレアやシアノグアニジンの生物学的等価性基としても注目されています。本研究室では、芳香属アミドやウレアの研究の展開として、スクアルアミドを鍵構造とした分子構築を行っており、結晶中および溶液中でらせん(図7、化合物6a等)7)や芳香族層状構造を形成する分子(図7、化合物6b,c等)8)や、外部環境の変化に応答して立体構造を変化させる分子スイッチの構築、液晶分子(図8、化合物7等)9)への展開などを行なっています。
7) Kanda, M. et al. Tetrahedron. 2019, 75, 2771-2777.
8) Arimura, M. et al. Chem. Plus Chem. 2021, 86, 198-205.
9)Park, S. et al. Chem. Lett. 2018, 47, 601-604
2.核内受容体を分子標的とした医薬化学研究
核内受容体は、ステロイドホルモンや脂溶性ビタミン等の脂溶性低分子化合物が結合して初めて特異的遺伝子発現の制御を行うリガンド依存的転写因子であり、分化、発生、代謝などの重要な生命現象を厳密に調整しています。また近年、核内受容体が癌、骨粗鬆症、糖尿病、動脈硬化など様々な疾患の発症と治療に関わっていることが示され、薬剤開発における重要な分子標的と考えられています。本研究室では、アミドおよび関連化合物で培った構造特性も活かしながら、新たな核内受容体リガンドの分子設計を行っています。
1)アンドロゲン受容体(AR)およびプロゲステロン受容体(PR)アンタゴニストの創製
私たちは、従来のリガンド構造とは骨格の異なるステロイドホルモン受容体リガンドを創製してきました。PRリガンドとして、蛍光センサーからヒントを得て、クマリン環に着目し、分子設計を行い、その中からプロゲステロン受容体(PR)アンタゴニスト8(図9)を見いだしました10)。本化合物をもとに、研究室の芳香族アミド研究で得たシス型アミド構造の立体特性を組み合わせて分子設計した結果、クマリン環をファーマコフォアとするアンドロゲン受容体(AR)アンタゴニスト9を見いだしました11)。更に、アミドをスルフォンアミドに代替することで、再びプロゲステロン受容体(PR)アンタゴニスト10にスイッチすることを見いだしました。最近では、クマリン環からキノロン環へ変換することで活性増強が見られることもわかり、非ステロイド型リガンドとして、独自の構造ライブラリーを構築しています。
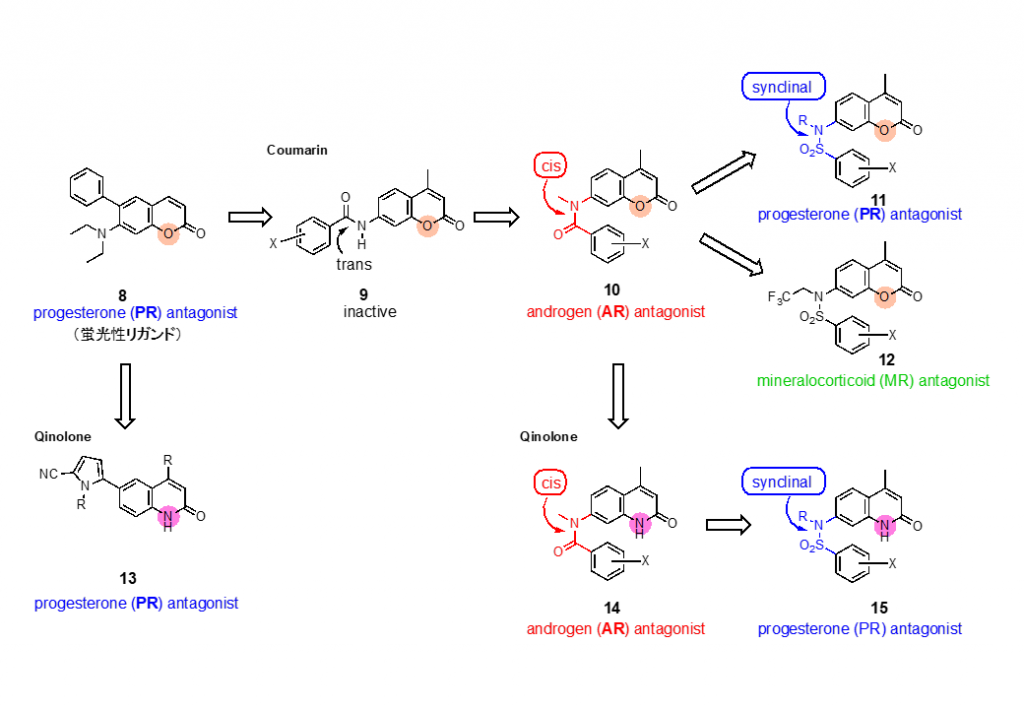
10) Sakai, H. et al. J. Med. Chem., 2011, 54, 7055-7065.
11) Koga, H. et al. Int. J. Mol. Sci., 2020, 21, 5584.
2)胆汁酸をリードとした高活性非セコステロイド型ビタミンD誘導体の創製
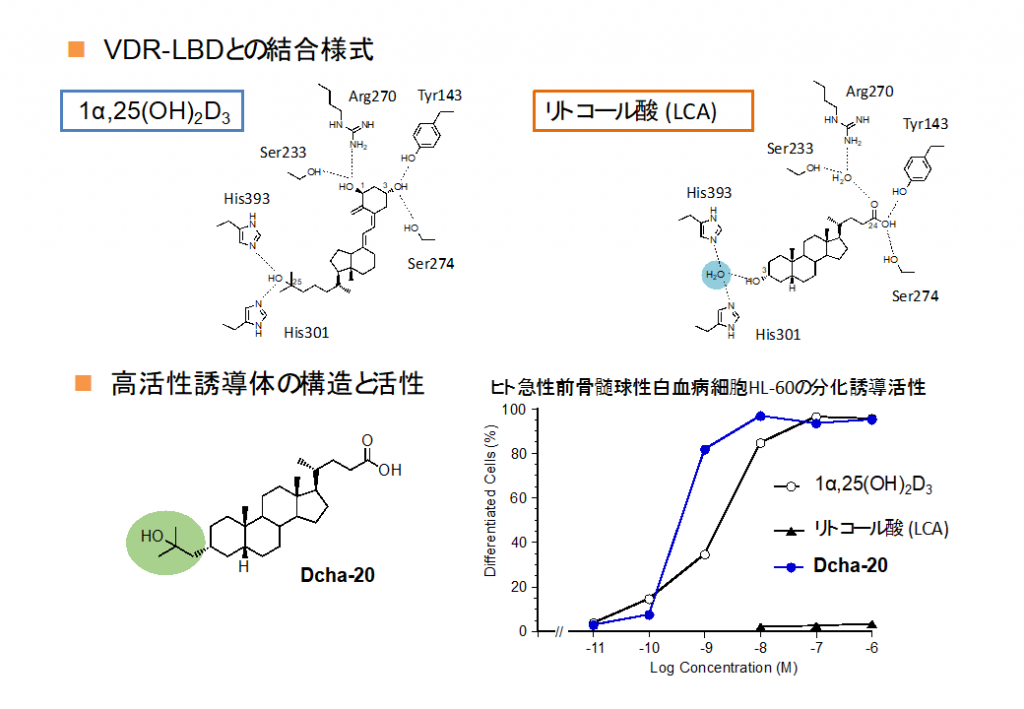
ビタミンDは、生体内で代謝されて活性本体である1a,25(OH)2D3となり、ビタミンDの核内受容体(VDR)に結合することにより特異的な遺伝子の発現を制御して、血中のカルシウム濃度維持や骨形成、免疫機能、細胞の分化・増殖制御などの重要な生理作用を担っています。これまでに、がん、骨粗鬆症などの疾患治療薬への応用を目的に多くのビタミンD誘導体が創製されてきましたが、医薬品になった化合物も含め、高活性な誘導体はいずれも天然型ビタミンDと同じセコステロイドとよばれる構造を持っていました。近年、セコステロイド構造を持たない高活性ビタミンD誘導体が報告されましたが、その数は限られています。
2002年にVDRの第2の内因性アゴニストとしてリトコール酸が見いだされましたが、その活性は1a,25(OH)2D3と比べると非常に弱いものでした。私たちは、リトコール酸とVDRの複合体の結晶構造をもとに高いビタミンD活性を持つリトコールさん誘導体Dcha-20の創製に成功しました(図10)12)。現在、Dcha-20の医薬応用を図るとともに、さらなる構造展開を行っています13)。
12) Sasaki, H. et al. J. Med. Chem. 2021, 64, 516-526.
13) Yoshihara, A. et al. Biomol. 2022, 12, 130.
